【香港商報網訊】記者 宋健 報導:9月28日,再鼎醫藥有限公司 (香港聯交所股票代碼:9688,NASDAQ:ZLAB)宣佈,正式在香港聯合交易所有限公司(「香港聯交所」)主板正式掛牌上市。再鼎醫藥本次全球發售共10,564,050股股份(未計及行使任何超額配股權),預計全球發售所得款項淨額約59.4億港元。由此,再鼎醫藥正式成為首個在香港二次上市的生物製藥公司。

再鼎醫藥創始人、董事長兼執行長杜瑩博士表示,本次香港上市,是再鼎醫藥成為世界領先醫藥公司願景的重要一步,展望未來,再鼎醫藥將進一步擴展藥物管線,尋求加速後期臨床資產審批和商業化、推進其他臨床或IND階段的候選藥物完成開發,持續為公司的股東及投資者帶來良好的回報。
據悉,2018年4月,香港聯交所開始實行上市新規則,新增生物科技公司章節(第18A章)。是次再鼎醫藥的上市亦標誌着,其成為繼香港上市新規則後首家在港二次上市的納斯達克生物醫藥公司。自2017年9月納斯達克上市至今,再鼎醫藥先後被納入,包括納斯達克生物技術指數(NBI)、MSCI全中國指數等多個重要核心成分指數。

成立僅六年,再鼎醫藥已迅速發展成為一家立足中國、全球運營的創新型生物製藥公司。憑藉自主研發和外部合作,再鼎醫藥打造起中國創新生物技術公司中最強大的晚期腫瘤產品管線,擁有多個全球同類首個或同類最佳藥物,在中國和全球各地發現、開發、生產並商業化創新藥物,成為了業界最值得信賴的合作夥伴人選之一。
自創立之初,公司就聚焦腫瘤、抗感染及自體免疫三大疾病領域,致力於為患者帶來突破性的創新藥物。目前產品管線中包括16種具有潛在全球同類最佳/同類首創潛力的產品及候選藥物。其中,兩款產品卵巢癌創新藥則樂及全球首款腫瘤電場治療產品愛普盾已在中國內地和港澳地區上市,另外,管線中還有九款產品處於關鍵或潛在註冊臨床研究階段,其中兩項已成功向中國國家藥監局遞交新藥上市申請(NDA)並獲得優先審評資格。
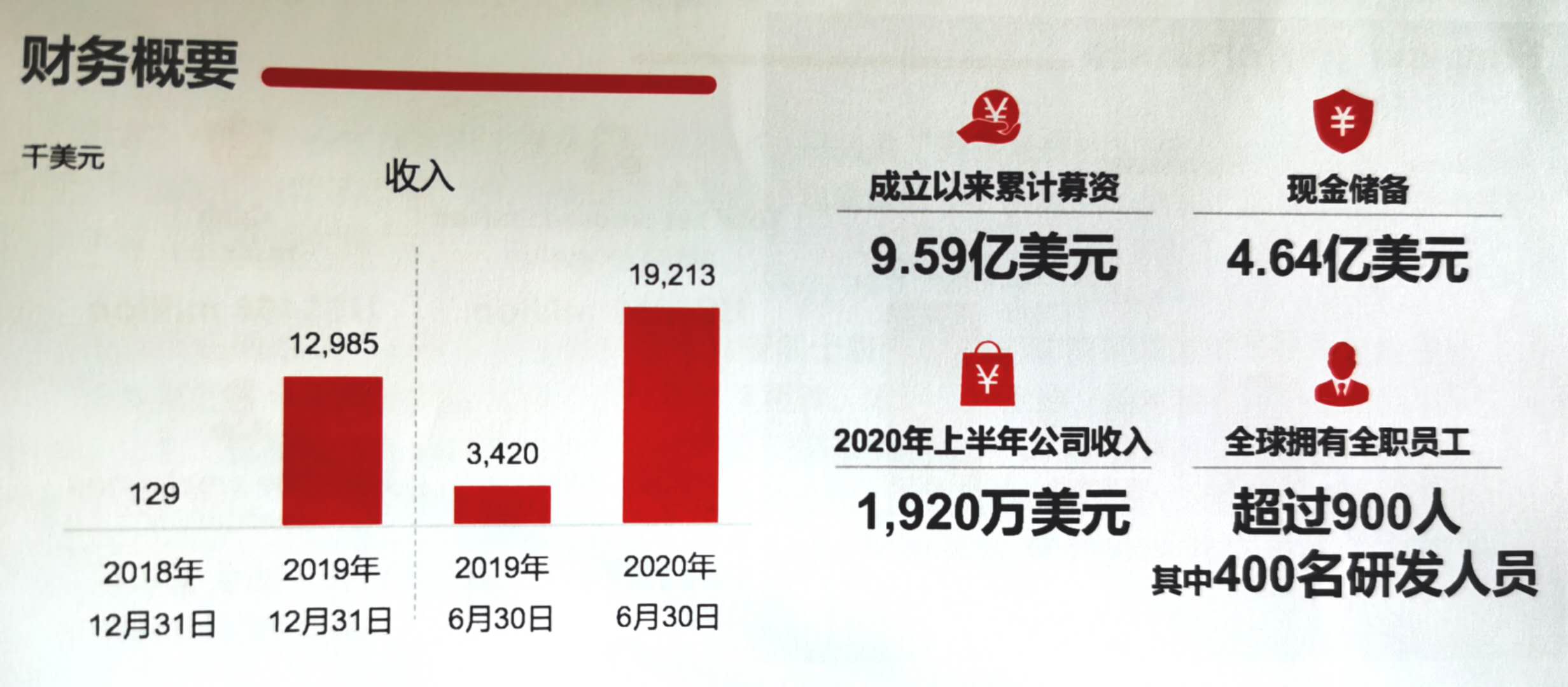
記者了解到,在新冠疫情肆虐全球的背景下,再鼎醫藥今年繼續實現跨越式的發展。今年5月,愛普盾在中國內地獲批用於新發和復髮膠質母細胞瘤的治療,成為15年來首個在國內獲批用於膠質母細胞瘤的創新療法;9月,則樂用於卵巢癌一線維持治療的補充新藥申請獲批,成為目前唯一獲批用於卵巢癌全人群一線維持治療的PARP抑制劑;今年,甲苯磺酸奧馬環素和瑞派替尼的上市申請獲受理並獲得了優先審評資格,其中甲苯磺酸奧馬環素用於治療社區獲得性細菌性肺炎 (CABP)及急性細菌性皮膚和皮膚結構感染(ABSSSI),瑞派替尼用於治療已接受過包括伊馬替尼在內的3種及以上激酶抑制劑治療的晚期胃腸道間質瘤(GIST)成人患者,並且已在今年7月成為海南自貿港博鰲樂城首個特批帶離藥物。
另外,今年再鼎醫藥與兩個全球性生物醫藥公司達成了同類最優的重磅產品的授權引進;上半年有20個臨床研究申請獲批,25個臨床研究正在計劃或進行中。兩款內部研發產品也進入全球臨床階段並實現了患者首次給藥。
本次發行上市,再鼎醫藥還將授予國際承銷商超額配股權,即承銷商可於9月22日之後的30天內可要求公司以發行價額外發行最多1,584,600股新股。
據了解,是次募集的資金將主要用於加強產品管線相關的臨床開發和內部研發工作,推進正在進行中和計劃中的臨床試驗,提升包括則樂和愛普盾在內的商業化能力,以及探索新的全球授權及合作機會,此外還將用於在全球招聘及培訓高端人才等,支持再鼎醫藥在中國和全球各地發現、開發、生產並商業化創新藥物,進一步擴大公司規模和影響力。


